Analisis Gaya Gesekan dan Gaya Berat

1. Gaya Gesekan
Gaya gesekan selalu memiliki arah yang berlawanan dengan arah gerak benda.

Kekasaran atau kehalusan permukaan suatu benda dapat mempengaruhi terhadap gaya gesek yang ditimbulkan.





| Waktu (sekon) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Jarak (meter) | 0 | 15 | 30 | 45 | 60 | 75 | 90 | 105 |




Besaran
|
Satuan
|
Lambang Satuan
|
Panjang
|
meter
|
m
|
Massa
|
kilogram
|
kg
|
Waktu
|
sekon
|
s
|
Kuat arus listrik
|
ampere
|
A
|
Suhu
|
kelvin
|
K
|
Jumlah zat
|
mol
|
mol
|
Intensitas cahaya
|
kandela
|
cd
|








Termometer
Klinis |
|
| Termometer klinis sering digunakan untuk mengukur suhu tubuh.
Umumnya, termometer ini digunakan oleh para dokter untuk mengetahui suhu
badan pasiennya. Termometer ini mempunyai skala dari 35 °C sampai dengan 42
°C. Hal ini dikarenakan suhu tubuh manusia tidak pernah kurang dari 35 °C
atau tidak pernah lebih dari 42 °C. Bagian-bagian termometer ini terdiri atas
tabung (terbuat dari kaca tipis), bagian sempit, batang kaca, dan air raksa. | |


 adalah panjang pada suhu t,
adalah panjang pada suhu t,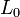 adalah panjang pada suhu awal,
adalah panjang pada suhu awal, adalah koefisien muai panjang, dan
adalah koefisien muai panjang, dan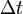 adalah besarnya perubahan suhu.
adalah besarnya perubahan suhu.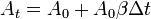
| No | Nama Basa | Rumus Kimia |
| 1 | Natrium hidroksida | NaOH |
| 2 | Amoniak | NH3 |
| 3 | Kalium oksida | K2O |
| 4 | Aluminium hidroksida | Al(OH)3 |




AHCI, dan XP dengan SATA Mode IDE/COMPABILITY) sebenarnya soal dumping Memori/Driver tidak ada hubungan dengan Mode hardisk.xiixiixixixi.

Dapatkan 3 unit mobil jenazah! Dan tiket emas liburan ke neraka. Ayo!! buruan kirimkan nyawa anda !! Makin banyak Dosa…. Makin besar kesempatan untuk disiksa !!.
